Введение в биомаркеры
Рабочая группа по определению биомаркеров определяет биомаркеры (биологические маркеры) как «измеримый индикатор состояния или процесса организма, который объективно измеряется и оценивается для исследования нормальных биологических процессов, патологических процессов или фармакологических реакций на терапевтическое вмешательство». Биомаркеры могут использоваться как диагностический инструмент, инструмент для оценки стадии заболевания, прогнозирования или для предсказания и мониторинга клинического ответа на вмешательство.[1] Биомаркеры могут иметь молекулярные, гистологические, радиографические или физиологические характеристики.[2]
Биомаркеры и болезнь Паркинсона
В зависимости от их характеристик биомаркеры болезни Паркинсона (ПБ) могут быть классифицированы на три основные категории[3][4][5]:
- Клинические
- Биохимические
- Нейровизуализация
1. Клинические биомаркеры
Двигательные признаки ПБ
К ним относятся кардинальные признаки ПБ, такие как тремор покоя, брадикинезия или акинезия, ригидность (в виде свинцовой трубы или зубчатого колеса) и постуральная нестабильность.[3] Среди них брадикинезия наиболее коррелирует с дегенерацией дофаминергических нейронов в нигростриарной системе.[5]
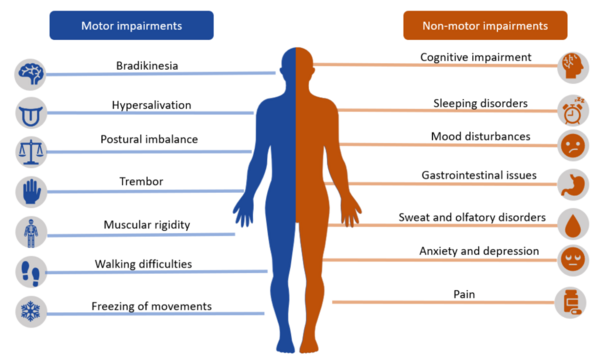
Недвигательные признаки ПБ
К ним относятся идиопатическое нарушение быстрого движения глаз (REM) [характеризующееся потерей атонии во время REM сна], гипосмия или аносмия (нарушается очень рано в ходе развития заболевания; также важно отметить, что, несмотря на это, не является специфичным для ПБ, оно относительно редко встречается у тех, у кого есть вторичный паркинсонизм), и запоры (опять же не специфичны для ПБ в изоляции, но их наличие в сочетании с потерей обоняния и нейровизуализацией может позволить более обоснованной диагностике ПБ).[3]
Все вышеупомянутые признаки могут идентифицироваться/количественно оцениваться с помощью клинических рейтинговых шкал, таких как шкала Хена и Яра (H&Y), Единая шкала болезни Паркинсона (UPDRS), шкала недвигательных симптомов болезни Паркинсона (NMSS) и Вопросник по болезни Паркинсона (PDQ-39) среди многих других.[3]
2. Биохимические биомаркеры
На основе телесных жидкостей и тканей
Альфа-синуклеин: Это основной компонент телец Леви и считается патологическим маркером ПБ.[3] Он может быть обнаружен в крови, цереброспинальной жидкости, слюне, моче, а также в желудочно-кишечном тракте.[5]
Окислительный стресс: Поскольку ПБ является нейродегенеративным заболеванием, признаки окислительного стресса можно обнаружить в центральной нервной системе. Это можно выявить по присутствию 8-гидроксидезоксигуанозина (8-OHdG), нитротирозина и реактивных форм кислорода.[3]
Мочевая кислота: Это потенциальный антиоксидант или поглотитель свободных радикалов. В животных моделях было выявлено, что она предотвращает гибель клеток в дофаминергических нейронах. Уровни мочевой кислоты значительно ниже в черной субстанции у лиц с ПБ.[3]
Генетические
Паркин (PARK2): Обычно встречается у лиц с ювенильной формой ПБ (возраст до 20 лет), аутосомно-рецессивным вариантом ПБ.[3]
Лейцин-обогащенная повторяющаяся сериновая киназа 2 (LRRK2): Встречается в аутосомно-доминантном варианте ПБ, наиболее распространенном среди представителей кавказской расы, но также был обнаружен у относительно небольшой части ашкеназских евреев и североафриканских арабов.[3]
Глюкоцереброзидаза: Сильно ассоциируется с началом заболевания ПБ.[3]
3. Нейровизуализационные биомаркеры
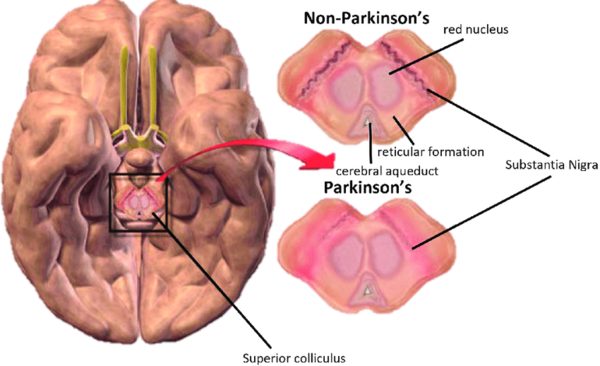
Радиотрейсерное изображение: Сканирование нигростриарной системы может быть использовано для обнаружения признаков паркинсонизма. Однако, оно очень дорогое и не специфично для ПБ.[3]
Транскраниальное ультразвуковое исследование (TCUS): Это может выявить гиперэхогенную черную субстанцию, которая коррелирует с значительно более высоким содержанием железа. Эта техника требует большого технического мастерства и дорогая.[3]
Магнитно-резонансная томография (МРТ): Она может показать изменения в диффузионно-тензорной томографии (DTI) каудального отдела черной субстанции. Эта техника тоже очень дорогая.[3]
Использование в исследованиях по физиотерапии
Оральные биомаркеры нейропластичности, вызванной упражнениями, при болезни Паркинсона
Альфа-синеклеопатии или аномальное выражение белка альфа-синуклеина, характерно встречающееся в стволе мозга у лиц с болезнью Паркинсона, также могут быть обнаружены в слюне. Симпатическая и парасимпатическая иннервации поднижнечелюстных желез, как утверждается, ответственны за эту трансдукцию через центральную нервную систему.[6]
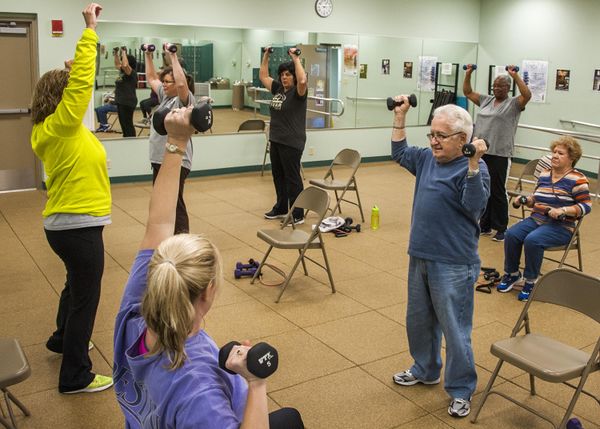
Кроме того, следующие оральные биомаркеры были обнаружены как увеличивающиеся в ответ на упражнения[6]:
- Нейротрофический фактор, происходящий из мозга (BDNF)
- Каталаза (CAT)
- Допаминовый рецептор D2 (DRD2)
- Глиальный клеточный нейротрофический фактор (GDNF)
- Глиальный фибриллярный кислый белок (GFAP)
- Глутаматный ионотропный рецептор типа AMPA подтип 2 (GRIA2)
- Синтаза оксида азота 2 (NOS2)
- Супероксиддисмутаза (SOD1)
- Сосудистый эндотелиальный фактор роста А (VEGFA)
Большинство этих данных ограничено исследованиями на животных с относительно ограниченными исследованиями на людях.[6] Это развивающаяся область исследований, и её результаты предоставят дополнительные доказательства роли упражнений при болезни Паркинсона.
Носимые сенсоры как цифровые биомаркеры болезни Паркинсона
Собранные данные с носимых сенсоров во время выполнения теста «Встать и идти» (TUG) изучались для прогноза частоты падений у лиц с болезнью Паркинсона. Авторы использовали Количественный тест «Встать и идти» (QTUG™), в котором беспроводной инерциальный сенсор крепится к одной из ног. Необходимо дальнейшее исследование для валидации этих результатов на большей популяции, особенно в клинических условиях.[7]
Это видео демонстрирует оборудование и выполнение Количественного теста «Встать и идти» (QTUG™).[8]
Ссылки
- ↑ Biomarkers Definitions Working Group. Биомаркеры и суррогатные конечные точки: предпочтительные определения и концептуальная схема. Clin Pharmacol Ther. 2001 Mar;69(3):89-95.
- ↑ Группа по работе с биомаркерами FDA-NIH. BEST (Биомаркеры, Конечные точки и другие инструменты) Ресурс [Интернет]. Silver Spring (MD): Food and Drug Administration (US); 2016 Jan 28 [Обновлено 2021 Nov 29].
- ↑ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 3.10 3.11 3.12 Morgan JC, Mehta SH, Sethi KD. Биомаркеры при болезни Паркинсона. Curr Neurol Neurosci Rep. 2010 Nov;10(6):423-30.
- ↑ Sharma S, Moon CS, Khogali A, Haidous A, Chabenne A, Ojo C, Jelebinkov M, Kurdi Y, Ebadi M. Биомаркеры при болезни Паркинсона (недавнее обновление). Neurochem Int. 2013 Sep;63(3):201-29.
- ↑ 5.0 5.1 5.2 Delenclos M, Jones DR, McLean PJ, Uitti RJ. Биомаркеры при болезни Паркинсона: достижения и стратегии. Parkinsonism Relat Disord. 2016 Jan;22 Suppl 1(Suppl 1):S106-10.
- ↑ 6.0 6.1 6.2 Mougeot JL, Hirsch MA, Stevens CB, Mougeot F. Оральные биомаркеры при нейропластичности, индуцированной физическими упражнениями, при болезни Паркинсона. Oral Dis. 2016 Nov;22(8):745-53.
- ↑ Greene BR, Premoli I, McManus K, McGrath D, Caulfield B. Прогнозирование числа падений с использованием носимых датчиков: новый цифровой биомаркер для болезни Паркинсона. Sensors. 2021 Dec 22;22(1):54.
- ↑ Kinesis QTUG - Количественное измерение времени в процессе встать-и-идти - инструкционное видео HD. Доступно по адресу: https://www.youtube.com/watch?v=WqbEfhSBxlQ (дата обращения: 23 мая 2022)
